 Управление по продуктам и лекарствам США (FDA) разрешило к применению на территории страны Cerena Transcranial Magnetic Stimulator (TMS) – портативное устройство для снятия симптомов мигрени, сопровождаемой аурой, сообщается в пресс-релизе ведомства.
Управление по продуктам и лекарствам США (FDA) разрешило к применению на территории страны Cerena Transcranial Magnetic Stimulator (TMS) – портативное устройство для снятия симптомов мигрени, сопровождаемой аурой, сообщается в пресс-релизе ведомства.
Cerena TMS, разработанный базирующейся в Калифорнии частной биотехнологической компанией eNeura Therapeutics, в настоящее время единственное применяемое в клинической практике устройство для немедикаментозной и неинвазивной терапии мигрени. В Великобритании этот аппарат под торговым наименованием Spring TMS с недавних пор доступен для пациентов старше 18 лет по специальному назначению лечащего врача в десяти специализированных клиниках. В США устройство планируется к применению по аналогичной схеме.
Принцип действия устройства основан на методе транскраниальной магнитной стимуляции, позволяющем неинвазивно стимулировать кору головного мозга при помощи коротких магнитных импульсов. Этот метод не сопряжен с болевыми ощущениями и широко применяется в качестве диагностической процедуры, например для оценки уровня связи моторной зоны коры и периферических мышц при инсульте, травмах позвоночника, рассеянном склерозе и боковом амиотрофическом склерозе.
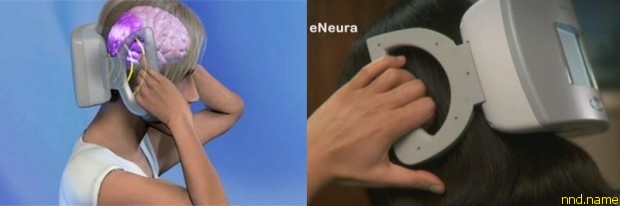
В начале приступа пациенту предлагается обеими руками прижать устройство к затылку и нажать кнопку. Короткий, длящийся одну миллисекунду, магнитный импульс при этом стимулирует затылочную кору с помощью слабых электрических токов, возбуждая и деполяризируя нейроны. Этот процесс нарушает связанную с началом приступа мигрени аномальную электрическую активность в головном мозге, полностью прекращая или снижая болевые ощущения. CerenaTMS автоматически записывает историю своего применения, занося ее в персональный «дневник головной боли».
Клинические испытания Cerena TMS, на результатах которых основывало свое решение FDA, показали, что применение устройства обеспечило двухчасовое избавление от боли после начала приступа у порядка 38 процентов из 113 участников, в то время как у контрольной группы этот эффект наблюдался лишь у 17 процентов. Через сутки около 34 процентов воспользовавшихся CerenaTMS все еще не испытывали болевых ощущений, в сравнении с 10 процентами участников контрольной группы.
В то же время, отмечается в пресс-релизе, испытания не показали эффективность устройства в отношении таких сопровождающих приступ мигрени с аурой симптомов, как гиперчувствительность к свету, звукам и тошнота. Среди побочных эффектов применения CerenaTMS отмечено головокружение, а также отдельные жалобы на синусит и афазию.
В FDA обращают внимание пациентов на недопустимость использования Cerena TMS в случае наличия в голове, шее или верхней части тела металла или действующего имплантируемого медицинского устройства, например кардиостимулятора. Кроме того, Cerena TMS нельзя применять пациентам с диагностированной или подозреваемой эпилепсией. Рекомендованный объем использования устройства не должен превышать одного раза в сутки.
В сентябре 2011 года в Евросоюзе был разрешен к применению имплантируемый электронейростимулятор Genesis, предназнаяенный для пациентов с хронической, устойчивой к терапии мигренью.
https://www.medlinks.ru/






