 Базовое редактирование гена SMN2 восстанавливает производство белка SMN, излечивая спинальную мышечную атрофию у мышей.
Базовое редактирование гена SMN2 восстанавливает производство белка SMN, излечивая спинальную мышечную атрофию у мышей.
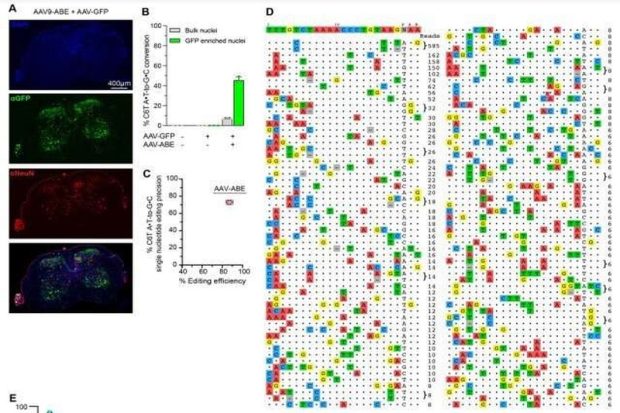
(A) Иммунофлуоресцентные изображения срезов спинного мозга мышей Δ7SMA дикого типа в возрасте 25 недель, которым вводили AAV9-ABE + AAV9-GFP в соотношении 10:1 путем неонатальной инъекции ICV, окрашенные на GFP для обозначения трансдукции AAV, NeuN в качестве маркера постмитотических нейронов и DAPI для окрашивания всех ядер.
(B) Преобразование C6T при редактировании оснований in vivo в спинном мозге мышей Δ7SMA, получавших AAV9-ABE + AAV9-GFP в объемной диссоциированной ткани и ядрах, обогащенных GFP+.
(C) Номинации CIRCLE-Seq потенциальных нецелевых сайтов в геномной ДНК клеток NIH3T3, обработанных in vitro очищенной нуклеазой Spy-mac и sgRNA P8. Несовпадения в каждом нецелевом локусе показаны относительно sgRNA выше.
(D) Целевое и нецелевое базовое редактирование стратегии D10 в мЭСК Δ7SMA. Столбцы показывают редактирование самого высокого редактируемого нуклеотида (P # показан в скобках) в каждом локусе.
(E) Флуоресцентная визуализация CND и MND дифференцированных Δ7SMAmESC, которые содержат репортер Mnx1: GFP моторных нейронов и стабильно интегрированы со стратегией ABE D10. (F) RT-qPCR для экспрессии ABE8e в Δ7SMAmESC (n = 3) и дифференцированных популяциях MND (n = 3) и CND (n = 3), ранее трансфицированных стратегией D10.
(G) Анализ экспрессии генов Δ7SMAmESC (n = 3) и дифференцированных клеток CND (n = 3) и MND (n = 3), показывающий уровни экспрессии различных двигательных нейронов, специфичных для нейронов, паттернов спинного мозга, глии и эмбриональных клеток. маркеры стволовых клеток. Кредит: ранее трансфицированных стратегией D10.
Анализ экспрессии генов Δ7SMAmESC (n = 3) и дифференцированных клеток CND (n = 3) и MND (n = 3), показывающий уровни экспрессии различных двигательных нейронов, специфичных для нейронов, паттернов спинного мозга, глии и эмбриональных клеток. маркеры стволовых клеток. Кредит: ранее трансфицированных стратегией D10.
Анализ экспрессии генов Δ7SMAmESC (n = 3) и дифференцированных клеток CND (n = 3) и MND (n = 3), показывающий уровни экспрессии различных двигательных нейронов, специфичных для нейронов, паттернов спинного мозга, глии и эмбриональных клеток. маркеры стволовых клеток. Кредит:Наука (2023). DOI: 10.1126/science.adg6518
Группа медицинских исследователей, связанных с множеством учреждений в США, использовала базовое редактирование, чтобы восстановить естественную выработку белка SMN у мышей, эффективно излечивая спинальную мышечную атрофию (СМА) у грызунов. В своей статье, опубликованной в журнале Science , группа описывает свой подход к базовому редактированию и его эффективность в восстановлении естественного производства SMN у мышей, страдающих СМА.
СМА является одной из ведущих причин младенческой смертности у людей. Дети, рожденные с этим заболеванием, имеют мутацию в гене SMN1, что приводит к выработке недостаточного количества белка SMN, что приводит к ухудшению состояния нервной системы и смерти. Многим детям, рожденным с этим заболеванием, у которых диагностировано достаточно рано, назначают препараты для искусственного увеличения производства SMN, что замедляет прогрессирование заболевания, но не может полностью остановить его. Таким образом, необходимы другие методы лечения.
В этой новой работе исследователи использовали базовое редактирование, своего рода редактирование генов, осуществляемое химическим путем, для лечения заболевания у мышей. Базовое редактирование обычно используется для внесения однонуклеотидных изменений в геном, как это было сделано в этом случае.
Запись лекции Дэвида Р. Лю по базовому редактированию и основному редактированию. Предоставлено: Дэвид Р. Лю.
В данном конкретном случае изменение было внесено в ген SMN2, который обычно частично кодирует производство SMN — изменения, внесенные командой, полностью активировали ген, что позволило увеличить производство SMN. Ген SMN2 связан с геном SMN1, но есть важное отличие: SMN2 имеет мутацию C6>T, которая делает его неспособным регулировать продукцию белка SMN. Изменение мутации таким образом, чтобы она стала идентичной немутированному гену SMN1, сняло это ограничение, позволив гену кодировать неограниченное количество SMN.
Тщательный мониторинг измененных мышей показал, что базовое редактирование восстановило производство SMN до нормального уровня, предотвратив дегенерацию нейронов. Они также обнаружили, что в тех случаях, когда дегенерация уже произошла, редактирование базы приводило к регенерации и улучшению двигательной функции. Они также обнаружили, что редактирование генов мышей увеличило продолжительность жизни в среднем с 17 дней (для контрольной группы) до более чем 100 дней.
Перевод: https://nnd.name/
Оригинал: https://medicalxpress.com/news/2023-03-base-smn2-gene-production-smn.html






