Компания Isis Pharmaceuticals недавно предоставила обновленные данные по клиническому исследованию препарата ISIS-SMNRx на детях со спинальной мышечной атрофией (СМА).
Компания Isis Pharmaceuticals недавно предоставила обновленные данные по клиническому исследованию препарата ISIS-SMNRx на детях со спинальной мышечной атрофией (СМА).
Текущее открытое многодозовое клиническое исследование второй фазы было направлено на исследование безопасности и переносимости препарата на 20 младенцах в возрасте до 7 месяцев, страдающих СМА первого типа.
Исследование продемонстрировало, что мышечная и моторная функции у детей, получивших препарат ISIS-SMNRx, усилилась. Результаты также свидетельствовали о том, что препарат продолжает хорошо переносится и, по-видимому, имеет положительный эффект в отношении прогрессирования заболевания.
Frank Bennett, доктор наук и старший вице-президент по научным исследованиям в компании Isis Pharmaceuticals, сообщил: «В этих исследованиях, которые используют множественные измерения изменений мышечных и моторных функции, мы наблюдали обнадеживающие результаты, которые сопоставимы с ранее полученными результатами нашего открытого исследования второй фазы. Эти данные, объединенные друг с другом, предполагают, что препарат ISIS-SMNRx мог бы принести выгоду пациентам с СМА помимо воспрепятствования прогрессирования заболевания. Данные по безопасности и переносимости препарата, которые мы наблюдаем во всех наших исследованиях ISIS-SMNRx, являются основание продолжения текущих программ третьей фазы на младенцах до 2 лет и детях старше 2 лет, страдающих СМА.
В настоящее время компания Isis проводит два дополнительных исследования третьей фазы препарата ISIS-SMNRx на младенцах и детях, страдающих СМА. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) присвоило препарату ISIS-SMNRx орфанный статус, а также статус приоритетного рассмотрения для лечения пациентов со СМА. В настоящее время компания Isis сотрудничает с компанией Biogen Idec по коммерциализации препарата ISIS-SMNRx.
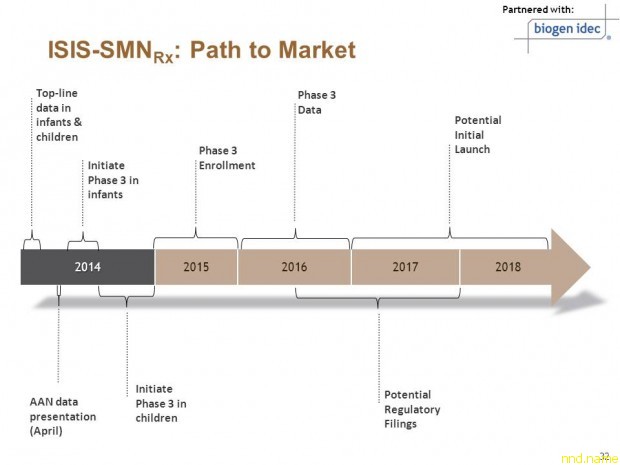
О препарате ISIS-SMNRx:
СМА вызвана мутациямив SMN1 гене. Это приводит к недостатку SMN белка (SMN protein)и ведет к выборочной атрофии (умиранию) нервных клеток, которые связывают спинной мозг с мышцами. Связь между нервными клетками и мышцами теряется и электрические сигналы более не могут быть переданы. Это, в свою очередь, ведет к атрофии мышц. В дополнение к SMN1 гену, существует еще второй ген, называемый SMN2 ген. Этот ген практически идентичен SMN1 гену за исключением одной буквы* в коде ДНК. Это ведет к образованию неполноценного белка, продуцированного с этого гена, который стремительно разрушается в клетках. Около 10 процентов функционального белка образуется с SMN2 гена.
*Буква – один из 4 нуклеотидов в составе ДНК — аденин (А), гуанин (Г), цитизин (Ц) и тимин (Т)
Препарат ISIS-SMNRx – это т.н. молекулярная заплатка, которая маскирует участок ДНК, отличающийся у SMN1 и SMN2 генов. Существует надежда, что таким путем с SMN2 гена может быть произведен полностью функциональный SMN белок.
https://f-sma.ru/